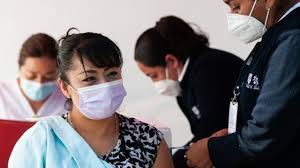
Martha Delgado, subsecretaria de Asuntos Multilaterales de la Secretaría de Relaciones Exteriores (SRE), informó en entrevista para Despierta que México recibirá 1.4 millones de vacunas contra COVID-19 en enero y 1.8 millones en febrero; “estamos en tiempo conforme a los contratos que la Secretaría de Salud firmó”, aseguró.
En la entrevista con Danielle Dithurbide y Enrique Campos, Martha Delgado detallo que hasta el momento México ha recibido 107 mil vacunas y que el próximo martes 12 de enero de 2021 llegarán 420 mil dosis más, en un solo lote.
La funcionaria dijo que la materia prima de la vacuna contra el COVID-19 de la farmacéutica CanSino podría llegar a nuestro país en las próximas semanas, para que sea envasada y esté disponible en febrero o a más tardar en marzo.
En cuanto a la vacuna de Moderna, que ya fue autorizada por la Administración de Medicamentos y Alimentos de Estados Unidos (FDA, por sus siglas en inglés), México tiene una propuesta de compra, pero no se ha concretado porque se podría surtir hasta junio o julio, “sin embargo, si la empresa puede hacer una dotación más tempranamente, seguramente el sector salud podrá valorarlo con mejores perspectivas”.
La funcionaria explicó que las cadenas de suministro de las vacunas contra la COVID-19 “están comprometidas a su máxima capacidad en todas las producciones… un lote que salga mal o que se eche a perder, en cualquiera de las fábricas de cualquier vacuna, puede retrasar puede retrasar en todo el mundo la llegada de la vacuna”.
Martha Delgado señaló que Rusia quiere hacer un ensayo clínico de Fase 3 de la vacuna Sputnik V en nuestro país, proceso que está en proceso de autorización en la Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris). Agregó que en la misma situación está la vacuna alemana CureVac.
“Yo creo que podemos ver un segundo tanda de contratos para vacunas para el segundo semestre del año 2021”, apuntó Martha Delgado.
¿Se puede adquirir la vacuna COVID-19 en el sector privado?
Cuestionada si las vacunas COVID-19 se pueden adquirir en el sector privado, la subsecretaria de Asuntos Multilaterales de la SRE subrayó que las autorizaciones de emergencia “son exclusivamente para uso gubernamental, esto es por el tipo de licencia que tienen; no es una licencia comercial”.
“Cuando terminen sus ensayos clínicos en Fase 3, como tienen que hacerlo durante el año 2021, pueden solicitar todas ellas su autorización de uso comercial y se podrían eventualmente poner a disposición del sector privado para la venta al público”, detalló.
Con información de Noticieros Televisa